Главная страница
 Базы данных
Базы данных
 База данных свойств веществ (поиск)
База данных свойств веществ (поиск)
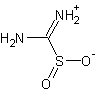
Свойства вещества:
тиомочевины диоксид
Синонимы и иностранные названия:
formamidinesulfinic acid (англ.)
формамидинсульфин (рус.)
формамидинсульфиновая кислота (рус.)
Тип вещества:
неорганическое
Внешний вид:
бел. кристаллыБрутто-формула (по системе Хилла для органических веществ):
CH4N2O2SФормула в виде текста:
(H2N)2SO2Молекулярная масса (в а.е.м.): 108,12
Температура плавления (в °C):
123Продукты термического разложения:
серы(IV) оксид; Растворимость (в г/100 г растворителя или характеристика):
ацетонитрил: практически не растворим [Лит.]
вода: 3 (20°C) [Лит.]
вода: 4,25 (31°C) [Лит.]
вода: 4,86 (35°C) [Лит.]
диметилсульфоксид: 2,29 (31°C) [Лит.]
диметилсульфоксид: 2,37 (35°C) [Лит.]
диметилсульфоксид: 2,65 (45°C) [Лит.]
диметилформамид: 0,1 (31°C) [Лит.]
диметилформамид: 0,11 (35°C) [Лит.]
диметилформамид: 0,12 (45°C) [Лит.]
нитрометан: практически не растворим [Лит.]
пропиленкарбонат: практически не растворим [Лит.]
тетрагидрофуран: практически не растворим [Лит.]
формамид: 2,18 (31°C) [Лит.]
формамид: 2,25 (35°C) [Лит.]
формамид: 2,65 (45°C) [Лит.]
этанол: 0,75 (20°C) [Лит.]
Вкус, запах, гигроскопичность:
гигроскопичен
Некоторые числовые свойства вещества:
Год открытия: 1910 (Барнет, окислением тиомочевины перекисью водорода)
Метод получения 1:
Источник информации: Бусев А. И. Синтез новых органических реагентов для неорганического анализа. - М.: Издательство московского университета, 1972 стр. 113К 230 мл 6%-ной водной перекиси водорода прибавляют постепенно в течение 1 часа 15 г растертой тиомочевины, все время охлаждая реакционную смесь в ледяной ванне. Тиомочевина растворяется. Через 1 ч формамидинсульфин выкристаллизовывается в форме бесцветных игл. Его отфильтровывают и извлекают непрореагировавшую тиомочевину кипящим этанолом, высушивают в вакууме над серной кислотой.
Выход 9 г.
Метод получения 2:
Источник информации: Шёнберг А. Препаративная органическая фотохимия. - М.: ИИЛ, 1963 стр. 117-1180,76 г тиомочевины (0,01 моля) в 100 мл этанола облучают в присутствии 50 мг красителя «бенгальская роза» при 20° в атмосфере О2. Для облучения применяют ртутную лампу высокого давления мощностью 125 вm (Osram HQA 500). За 20 мин поглощается 1 л кислорода. Благодаря выделению кристаллов уже через 14 мин наблюдается помутнение раствора. После отсасывания и промывания осадка теплым спиртом было получено 0,56 г вещества (60,2% от теоретического) с т. пл. 142—143° (плавится с разложением), которое идентично продукту, полученному из тиомочевины и 6%-ной Н2О2.
Способы получения:
- Диоксид тиомочевины легко получается окислением тиомочевины пероксидом водорода в нейтральной среде при 0-5 С. [Лит.1, Лит.2
 ]
]
Показатели диссоциации:
pKa (1) = 6,82 (25°C, вода)
Дополнительная информация::
Не образует кристаллогидратов. Способен долго храниться.
Восстанавливает альдегиды и кетоны до спиртов с выходом 75-100%. Реагирует с алкиламинами с образованием диоксидов N-алкилтиомочевин. Восстанавливает нитроарены до анилинов в щелочной среде, при большом избытке восстановителя. Восстанавливает сульфоксиды до сульфидов в присутствии иода (без иода реакция не идет) в ацетонитриле при 80 С с выходами более 90%.
Источники информации:
- CRC Handbook of Chemistry and Physics. - 95ed. - CRC Press, 2014. - С. 3-278
- Буданов В.В., Макаров С.В. Химия серосодержащих восстановителей (ронгалит, дитионит, диоксид тиомочевины). - М.: Химия, 1994
- Вредные вещества в промышленности: Справочник для химиков, инженеров и врачей. - 7-е изд., Т.2. - Л.: Химия, 1976. - С. 58
- Вредные вещества в промышленности: Справочник для химиков, инженеров и врачей. - 7-е изд., Т.2. - Л.: Химия, 1976. - С. 58
- Физер Л., Физер М. Реагенты для органического синтеза. - Т. 7. - М.: Мир, 1978. - С. 499
Если не нашли нужное вещество или свойства можно выполнить следующие действия:
Если вы нашли ошибку на странице, выделите ее и нажмите Ctrl + Enter.
© Сбор и оформление информации: Руслан Анатольевич Кипер